No cultivo hidropônico, a composição da solução nutritiva deve ser adequada ao tipo de vegetal que se pretende cultivar. Uma solução específica para o cultivo do tomate, por exemplo, apresenta as seguintes concentrações de macronutrientes:
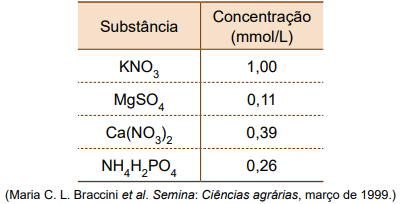
Durante o desenvolvimento das plantas, é necessário um rígido controle da condutividade elétrica da solução nutritiva, cuja queda indica diminuição da concentração de nutrientes. É também necessário o controle do pH dessa solução que, para a maioria dos vegetais, deve estar na faixa de 5,0 a 6,5.
a) Por que a solução nutritiva para o cultivo hidropônico de tomate é condutora de eletricidade? Calcule a quantidade, em mmol, do elemento nitrogênio presente em 1,0 L dessa solução.
b) Considere que 1,0 L de uma solução nutritiva a 25 ºC, inicialmente com pH = 6,0, tenha, em um controle posterior, apresentado o valor mínimo tolerável de pH = 4,0. Nessa situação, quantas vezes variou a concentração de íons H+ (aq)? Sabendo que o produto iônico da água, Kw, a 25 ºC, é igual a 1,0 × 10–14, calcule as quantidades, em mol, de íons OH– (aq) presentes, respectivamente, na solução inicial e na solução final.
a) Porque a solução nutritiva é salina, logo, contém íons livres.
Para 1 L de solução:
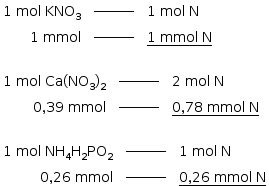
A quantidade do elemento N em um litro de solução é:
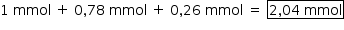
b)  Quando o pH da solução varia de 6 para 4, a concentração de íons H+ varia em 100 vezes, pois:
Quando o pH da solução varia de 6 para 4, a concentração de íons H+ varia em 100 vezes, pois:
 Quando o pH da solução varia de 6 para 4, a concentração de íons H+ varia em 100 vezes, pois:
Quando o pH da solução varia de 6 para 4, a concentração de íons H+ varia em 100 vezes, pois:![«math style=¨font-family:Tahoma¨ xmlns=¨http://www.w3.org/1998/Math/MathML¨»«mstyle mathsize=¨14px¨»«mrow»«mi»pH«/mi»«mo»§#xA0;«/mo»«mo»=«/mo»«mo»§#xA0;«/mo»«mn»4«/mn»«mo»§#xA0;«/mo»«mo»§#x21D2;«/mo»«mo»§#xA0;«/mo»«mfenced open=¨[¨ close=¨]¨»«msup»«mi mathvariant=¨normal¨»H«/mi»«mo»+«/mo»«/msup»«/mfenced»«mo»§#xA0;«/mo»«mo»=«/mo»«mo»§#xA0;«/mo»«msup»«mn»10«/mn»«mrow»«mo»-«/mo»«mn»4«/mn»«/mrow»«/msup»«mo»§#xA0;«/mo»«mfrac bevelled=¨true¨»«mi»mol«/mi»«mi mathvariant=¨normal¨»L«/mi»«/mfrac»«mspace linebreak=¨newline¨/»«mi»pH«/mi»«mo»§#xA0;«/mo»«mo»=«/mo»«mo»§#xA0;«/mo»«mn»6«/mn»«mo»§#xA0;«/mo»«mo»§#x21D2;«/mo»«mo»§#xA0;«/mo»«mfenced open=¨[¨ close=¨]¨»«msup»«mi mathvariant=¨normal¨»H«/mi»«mo»+«/mo»«/msup»«/mfenced»«mo»§#xA0;«/mo»«mo»=«/mo»«mo»§#xA0;«/mo»«msup»«mn»10«/mn»«mrow»«mo»-«/mo»«mn»6«/mn»«/mrow»«/msup»«mo»§#xA0;«/mo»«mfrac bevelled=¨true¨»«mi»mol«/mi»«mi mathvariant=¨normal¨»L«/mi»«/mfrac»«mspace linebreak=¨newline¨/»«mi»Raz§#xE3;o«/mi»«mo»§#xA0;«/mo»«mo»=«/mo»«mo»§#xA0;«/mo»«mfrac»«mrow»«msup»«mn»10«/mn»«mrow»«mo»-«/mo»«mn»4«/mn»«/mrow»«/msup»«mo»§#xA0;«/mo»«mstyle displaystyle=¨true¨»«mfrac bevelled=¨true¨»«mi»mol«/mi»«mi mathvariant=¨normal¨»L«/mi»«/mfrac»«/mstyle»«/mrow»«mrow»«msup»«mn»10«/mn»«mrow»«mo»-«/mo»«mn»6«/mn»«/mrow»«/msup»«mo»§#xA0;«/mo»«mstyle displaystyle=¨true¨»«mfrac bevelled=¨true¨»«mi»mol«/mi»«mi mathvariant=¨normal¨»L«/mi»«/mfrac»«/mstyle»«/mrow»«/mfrac»«mo»§#xA0;«/mo»«mo»=«/mo»«mo»§#xA0;«/mo»«mn»100«/mn»«mspace linebreak=¨newline¨/»«mi»Como«/mi»«mo»§#xA0;«/mo»«mfenced open=¨[¨ close=¨]¨»«msup»«mi mathvariant=¨normal¨»H«/mi»«mo»+«/mo»«/msup»«/mfenced»«mo»§#xA0;«/mo»«mo»§#xB7;«/mo»«mo»§#xA0;«/mo»«mfenced open=¨[¨ close=¨]¨»«msup»«mi»OH«/mi»«mo»-«/mo»«/msup»«/mfenced»«mo»§#xA0;«/mo»«mo»=«/mo»«mo»§#xA0;«/mo»«msup»«mn»10«/mn»«mrow»«mo»-«/mo»«mn»14«/mn»«/mrow»«/msup»«mo»,«/mo»«mo»§#xA0;«/mo»«mi»tem«/mi»«mo»-«/mo»«mi»se«/mi»«mo»:«/mo»«mspace linebreak=¨newline¨/»«mspace linebreak=¨newline¨/»«/mrow»«/mstyle»«/math»](https://anglo.plurall.net/sites/all/libraries/ckeditor//plugins/ckeditor_wiris/integration/showimage.php?formula=cff2bbb74611be379f639c735f299e18.png)
 Na solução inicial:
Na solução inicial:![«math style=¨font-family:Tahoma¨ xmlns=¨http://www.w3.org/1998/Math/MathML¨»«mstyle mathsize=¨14px¨»«mrow»«mfenced open=¨[¨ close=¨]¨»«msup»«mi mathvariant=¨normal¨»H«/mi»«mo»+«/mo»«/msup»«/mfenced»«mo»§#xA0;«/mo»«mo»=«/mo»«mo»§#xA0;«/mo»«msup»«mn»10«/mn»«mrow»«mo»-«/mo»«mn»6«/mn»«/mrow»«/msup»«mo»§#xA0;«/mo»«mfrac bevelled=¨true¨»«mi»mol«/mi»«mi mathvariant=¨normal¨»L«/mi»«/mfrac»«mo»,«/mo»«mo»§#xA0;«/mo»«mi»ent§#xE3;o«/mi»«mo»§#xA0;«/mo»«mfenced open=¨[¨ close=¨]¨»«msup»«mi»OH«/mi»«mo»-«/mo»«/msup»«/mfenced»«mo»§#xA0;«/mo»«mo»=«/mo»«mo»§#xA0;«/mo»«msup»«mn»10«/mn»«mrow»«mo»-«/mo»«mn»8«/mn»«/mrow»«/msup»«mo»§#xA0;«/mo»«mfrac bevelled=¨true¨»«mi»mol«/mi»«mi mathvariant=¨normal¨»L«/mi»«/mfrac»«mspace linebreak=¨newline¨/»«/mrow»«/mstyle»«/math»](https://anglo.plurall.net/sites/all/libraries/ckeditor//plugins/ckeditor_wiris/integration/showimage.php?formula=a3e6f27c900bd3e3660c344b19cfabf3.png)
 Na solução final:
Na solução final:![«math style=¨font-family:Tahoma¨ xmlns=¨http://www.w3.org/1998/Math/MathML¨»«mstyle mathsize=¨14px¨»«mrow»«mfenced open=¨[¨ close=¨]¨»«msup»«mi mathvariant=¨normal¨»H«/mi»«mo»+«/mo»«/msup»«/mfenced»«mo»§#xA0;«/mo»«mo»=«/mo»«mo»§#xA0;«/mo»«msup»«mn»10«/mn»«mrow»«mo»-«/mo»«mn»4«/mn»«/mrow»«/msup»«mo»§#xA0;«/mo»«mfrac bevelled=¨true¨»«mi»mol«/mi»«mi mathvariant=¨normal¨»L«/mi»«/mfrac»«mo»,«/mo»«mo»§#xA0;«/mo»«mi»ent§#xE3;o«/mi»«mo»§#xA0;«/mo»«mfenced open=¨[¨ close=¨]¨»«msup»«mi»OH«/mi»«mo»-«/mo»«/msup»«/mfenced»«mo»§#xA0;«/mo»«mo»=«/mo»«mo»§#xA0;«/mo»«msup»«mn»10«/mn»«mrow»«mo»-«/mo»«mn»10«/mn»«/mrow»«/msup»«mo»§#xA0;«/mo»«mfrac bevelled=¨true¨»«mi»mol«/mi»«mi mathvariant=¨normal¨»L«/mi»«/mfrac»«/mrow»«/mstyle»«/math»](https://anglo.plurall.net/sites/all/libraries/ckeditor//plugins/ckeditor_wiris/integration/showimage.php?formula=bd3284adc9f26fa04e2244a57c441337.png)
Para 1 L de solução, haverá 10–8 mol de OH– na solução inicial e 10–10 mol de OH– na solução final.







Nenhum comentário:
Postar um comentário